Le potentiel standard d'oxydo-réduction
1 Définitions
Le potentiel standard d’oxydoréduction est une grandeur exprimée en Volts (V) associée à un couple rédox. Il permet de situer le couple sur une échelle des couples rédox.
Par convention, on le verra, le couple H+/H2 est associé au potentiel V H+/H 2 = 0 V.
Petit rappel de physique chimie :
Pour ceux qui n’ont jamais réussi à comprendre la différence entre tension et intensité, on propose ici un schéma qui permet d’établir que la tension est bien une différence entre deux potentiels. La tension peut en effet être assimilée à la hauteur de la chute d’eau, qui est égale à la différence entre les altitudes (potentiels) de départ et d’arrivée. Cette tension est à distinguer de l’intensité qui peut être assimilée au débit de la chute d’eau qui ne dépend pas de la hauteur de la cascade mais seulement de la quantité d’eau disponible en amont de la cascade.
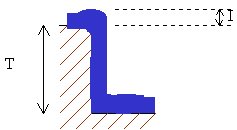
Remarque : Si le " bas " de la cascade se situe à l’altitude zéro, il est clair que la hauteur de la chute sera égale à l’altitude du haut de la cascade. On voit ici s’ébaucher l’intérêt de placer le couple H+/H2 à un potentiel égal à 0V.
On appelle demi-pile l’ensemble constitué par une plaque de métal et les ions correspondant à son conjugué en général en solution. Une demi-pile est donc celle d’un couple rédox et met en présence les deux conjugués. Pour plus de facilité, on notera Mn+/M un couple-type qui nous servira dans l’ensemble des développements suivants.
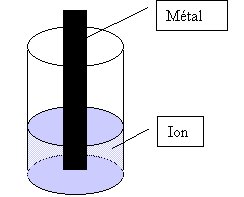
Une pile est formée de l’association de deux demi-piles différentes reliées entre elles pour permettre le passage des ions.
On peut utiliser deux moyens : soit on met en place un pont ionique qui consiste en une sorte de lamelle de papier absorbant imbibée d’une solution saline destinée à le rendre conducteur électriquement, soit on place entre les deux demi-piles une paroi poreuse laissant les ions transiter à travers elles. Dans les deux cas, le but est de créer un lien conducteur entre les deux demi-piles.
2 La pile d'oxydoréduction
2.1 Protocole
On construit une pile entre deux couples
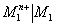 et. Lorsque le couple
et. Lorsque le couple
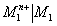 est celui qui a le potentiel le
plus fort, on note la pile en le plaçant en premier, suivi de l’autre couple, séparé par une double
ligne (en général, en pointillés).
est celui qui a le potentiel le
plus fort, on note la pile en le plaçant en premier, suivi de l’autre couple, séparé par une double
ligne (en général, en pointillés).
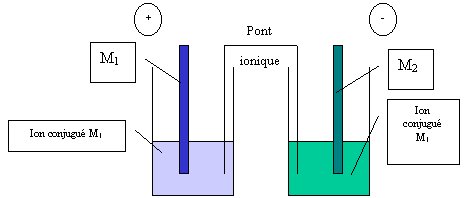
2.2 Observation
On observe qu’une tension se crée entre les deux électrodes, ce même si l’on place un voltmètre parfait ( c’est à dire sans résistance interne) entre les deux plaques métalliques. On en déduit qu’il existe une tension à vide entre les bornes de cette pile. On l’appelle aussi f.é.m. pour force électromotrice, notée e. On établit la relation e = VM2-VM1. Dans ce cas, on a e positive. (la f.e.m. est une grandeur toujours positive )
La pile ainsi formée est un générateur de tension. La borne + se trouve sur la plaque métallique correspondant à l’oxydant le plus fort. A l’inverse, c’est la plaque métallique constituée par le réducteur le plus fort qui constitue l’électrode -.
On constate donc une diminution de la masse de la plaque métallique constituant l’anode, c’est à dire celle du couple ayant le plus fort réducteur. A l’inverse, il y a disparition des ions dans la solution de la demi-pile correspondant à la borne +.
2.3 Analyse
On appelle anode l’électrode par laquelle le courant entre dans la pile. Il s’agit donc de la borne -, celle où se produit l’oxydation. En effet, le courant est un transfert d’électrons. On rappelle que par convention, le courant est orienté dans le sens contraire de celui des électrons. Lorsqu’il entre dans une borne, il y a donc sortie massive d’électrons. Ceux-ci doivent être libérés. On rappelle que la définition de l’oxydation est justement une perte d’électrons ( puisque c’est le réducteur qui subit l’oxydation et que ce dernier libère des électrons). Il y a bien oxydation sur l’anode.
De son côté, la cathode est l’électrode par laquelle sort le courant. Elle correspond donc à la borne +.Il s’agit donc de celle où se déroule la réduction. On sait par définition que la réduction est un gain d’électrons puisque c’est un oxydant qui est réduit et que ce dernier obtient des électrons.
On peut donc écrire les demi-équations qui se réalisent sur chacune des électrodes.
- Sur l’anode ( pole -) : M -> Mn+ + n e-
- Sur la cathode (pole +): Mn+ + ne- -> M
On est ici dans un cadre bien connu. Il n’est pas difficile de prévoir quelle sera la borne + et la borne – d’une pile avant même qu’elle ne soit mise en place. En effet, on peut appliquer la règle du gamma (moyen mnémotechnique ) aux demi-piles : celle qui jouera le rôle de la borne + sera logiquement celle dont le pouvoir oxydant est le plus fort tandis que le meilleur réducteur fera de sa demi-pile la borne -.
Les bornes sont constituées par les métaux qui sont tous deux réducteurs et non par
les couples. On confirme donc bien que si
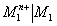 est le métal qui a le plus fort potentiel
oxydant, il est amené à être naturellement la borne +.
est le métal qui a le plus fort potentiel
oxydant, il est amené à être naturellement la borne +.
Certains paramètres influent sur la f.é.m. d’un pile. Il s’agit :
- la concentration des solutions ioniques ( dans lesquelles se trouvent les oxydants des deux couples)
- le pH des solutions ( parce que l’ion H+ peut jouer un rôle d’oxydant).
- la température
On définit donc des conditions standards qui permettent de rendre les observations comparables :
- concentration molaire des solutions ioniques : 1 mol.L-1.
- Pression des gaz : 1 bar ( on utilise la pression des gaz parce que certains réducteurs sont gazeux. C’est le cas pour H2.)
- La température est choisie arbitrairement.
3 Potentiel standard d'oxydoréduction
Demi-pile de référence
L’électrode standard à hydrogène (E.S.H.) est une électrode virtuelle en platine, plongée dans une solution de pH=0 et entourée de dihydrogène gazeux à la pression 1 bar. Elle réalise donc toutes les conditions standard, d’où son appellation de standard.
On l’utilise pour définir le potentiel d’oxydoréduction d’un couple Mn+/M : on appelle potentiel d’oxydoréduction d’un couple Ox1/Red1 la tension aux bornes des deux demi-piles en circuit ouvert. C’est donc la tension entre l’E.S.H. et la plaque métallique M.
On utilise le terme de potentiel standard d’oxydoréduction lorsque cette pile est réalisée dans les conditions standard d’expérimentation.
Il résulte de cette définition que le potentiel standard d’oxydoréduction du couple H+/H2 est nul. En effet, la tension entre deux E.S.H. sera logiquement nulle : si l’on veut utiliser la règle du gamma, on constate qu’il est impossible de tracer le gamma sir une échelle avec le seul couple H+/H2. En réalité, si une réaction était possible dans un sens, elle le serait aussi dans l’autre et il y a automatiquement une neutralisation des deux conjugués du couple.
Demi-pile de référence secondaire
On utilise des demi-piles de référence secondaires dont on connaît le potentiel d’oxydoréduction pour déterminer les potentiels standards d’autres couples.
En reprenant le schéma de la cascade présenté plus haut, on comprend bien que la détermination est possible dès lors que l’on connaît la tension entre la demi-pile du couple testé et celle de référence secondaire ( c’est à dire leur différence d’altitude) dès lors que l’on connaît le potentiel de la demi-pile de référence secondaire ( son altitude sachant que celle du couple H+/H2 est 0).
En réalité, on peut utiliser une sorte de relation de Chasles pour déterminer le potentiel d’un couple à partir de celui d’un couple connu et de la f.é.m. d’une pile les réunissant.
On retient la demi-pile de référence faisant intervenir le couple Cu2+/Cu dont on connaît le potentiel : 0,34 V.
Le potentiel standard du couple Mn+/M se note de la façon suivante :
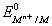 et s’exprime en Volts.
et s’exprime en Volts.
Le potentiel d’un couple est positif dès que les cations sont un oxydant plus fort que H+ et négatif dès lors que M est plus réducteur que H2.
Plus le potentiel d’oxydation est fort, plus l’oxydant du couple l’est et moins fort est son réducteur.
La f.é.m. d’une pile est égale à la différence entre le potentiel standard rédox du couple dont l’oxydant est le plus fort et celui du couple dont l’oxydant est le plus faible. Elle est donc toujours positive.
Les difficultés de la leçon
Il faut bien connaître son cours sur l’oxydo-réduction pour connaître les définitions.
Il faut maîtriser :
- les définitions de anode, cathode, réducteur, oxydant, oxydation, réduction
- leur répartition entre les deux demi-pile
- la définition du potentiel standard et son utilisation