Les couples d'oxydo-réduction
1 Définitions
Une oxydoréduction est une réaction au cours de laquelle s’effectue un transfert d’électrons entre deux espèces chimiques.
- Le réducteur cède des électrons : il subit une oxydation.
- L’oxydant capte des électrons : il subit une réduction.
Il faut parvenir à mémoriser correctement ces définitions. On propose un moyen mnémotechnique :
- Le Réducteur Rend des électrons. L’Oxydant en Obtient.
Un couple rédox ou oxydant réducteur est constitué par l’ensemble formé par l’oxydant et le réducteur d’un seul et même élément. On le note en juxtaposant les abréviations de l’oxydant et du réducteur séparés par un /. Par exemple le couple du cuivre est noté Cu2+/Cu où Cu2+ est l’oxydant et Cu est le réducteur. La deuxième partie d’un couple rédox est aussi appelé conjugué : Cu est le réducteur conjugué du Cu2+.
On représente les passages de l’un à l’autre grâce à une double flèche
 qui
indique que la réciproque est aussi vraie. On a ainsi :
qui
indique que la réciproque est aussi vraie. On a ainsi :
- Réducteur
 Oxydant + n e-
Oxydant + n e-
2 Réaction d'oxydoréduction
C’est une réaction de transfert d’électrons qui fait intervenir deux couples rédox. L’oxydant de l’un va capter les électrons que cède le réducteur de l’autre. Il y a donc à la fois oxydation et réduction d’où le nom de la réaction.
On construit l’équation–bilan de cette réaction en additionnant les deux demi-équations des
réactifs entre elles.
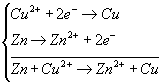
On peut par ailleurs être amené à affecter un coefficient à l’une ou l’autre de ces demi-équation
pour garantir qu’il ne reste pas d’électron libre esseulé. Par exemple :
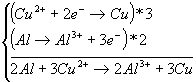
On constate ici qu’il y a bien une égalité du nombre total de charges de part et d’autres de l’équation –bilan de la réaction.
3 Classification qualitative des couples rédox
L’observation de la réalité permet de constater que les couples rédox ne réagissent pas n’importe
quoi. On s’attendrait en effet à avoir aussi bien 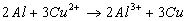 . Pourtant, l’observation montre que ce n’est
pas le cas.
. Pourtant, l’observation montre que ce n’est
pas le cas.
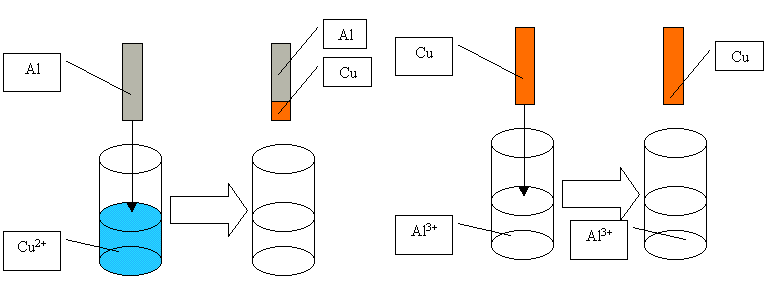
La première réaction fonctionne manifestement : il y a décoloration de la solution cuivrée et du cuivre métallique apparaît sur l’aluminium qui se fait ronger. A l’inverse, la deuxième expérience ne débouche sur aucune réaction. On peut en déduire que Cu2+ est plus facilement oxydant que ne l’est Al3+. De même l’aluminium sous sa forme métallique semble être un réducteur plus efficace.
On peut donc évaluer quantitativement chacun des couples rédox en fonction de leur pouvoir
oxydo-réducteur. Il semble d’ailleurs clair que pour un couple donné, plus son oxydant est fort
plus son conjugué a un pouvoir réducteur faible. On peut donc placer chaque couple sur une double
échelle qui permet de prédire quelle sera la tendance d’un couple : réagir plutôt comme oxydant
ou plutôt comme réducteur. Dans notre exemple, on peut établir le schéma suivant :
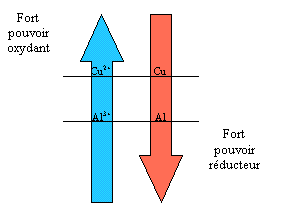
On remarque alors que la réaction effective n’existe que dan un seul sens : celui qui place les réactifs sur la diagonale d’en haut vers la droite. On généralise cette observation par la règle du gamma que nous verrons plus loin.
4 Généralisation
On peut généraliser en utilisant un couple de référence et en cherchant à classer chaque couple rédox par rapport à cet indicateur et par rapport aux autres couples.
Le couple choisi comme référence est le couple H+/H2 qui constituera donc le zéro de l’échelle des couples que l’on cherche à construire.
En complétant l’échelle, on peut petit à petit parvenir à prévoir les réactions qui auront naturellement lieu et celle qui au contraire sont impossibles dans un contexte normal. Pour ce, on utilise la règle appelée règle du gamma qui consiste à observer que la réaction naturelle est celle qui place les réactifs sur la diagonale du haut vers la droite. On appelle cette règle "règle du gamma" parce que les réactifs et les produits se placent sur deux branches de la lettre grecque gamma et qu’en traçant la lettre de façon imaginaire sur l’ échelle des couples, on peut voir apparaître la réaction qui sera possible :
Moyen mnémotechnique à utiliser comme tel et à ne pas ériger en loi !
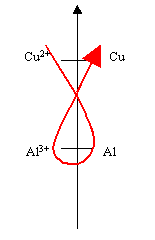
Cette règle du gamma permet, dès lors que l’on dispose d’une échelle des potentiels rédox de prévoir quelle va être la réaction naturelle possible et laquelle sera impossible.
Les présentations de ces échelles varient souvent mais on a toujours les oxydants placés sur la gauche et le pouvoir oxydant est croissant sur le schéma, les couples ayant les plus forts potentiels oxydants étant placés en haut de l’échelle.
Il faut bien sur retenir que le couple H+/H2 est le couple de référence. On peut dès lors observer que l’ion H+ caractéristique des solutions acides ne peut pas oxyder tous les métaux. Il est pas exemple incapable de réagir avec le cuivre métallique alors que le cuivre peut être obtenu par réaction entre le Cu2+ et le dihydrogène.
La lecture de cette échelle permet par ailleurs de mieux comprendre pourquoi certains métaux ne peuvent être que difficilement trouvés dans la nature à l’état métallique mais le sont plutôt sous forme d’un minerai constituant en un composé ionique.
On peut prendre l’exemple de l’aluminium. Il s’agit d’un métal qui a un très grand pouvoir
réducteur. On peut le placer sur une échelle des potentiels rédox de la façon suivante :
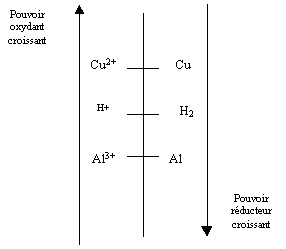
Cette échelle permet de voir que la réaction de l’aluminium métallique est notamment possible avec l’ion H+, typique du milieu acide et qui est extrêmement répandu. L’aluminium métallique a donc largement tendance à réagir et on a plutôt tendance à trouver le conjugué de Al : Al3+, notamment dans l’alumine. Il apparaît à l’inverse que certains métaux seront plus faciles à trouver dans les gisements naturels sous forme métallique.
Les difficultés de la leçon
Il faut savoir :
- équilibrer une équation bilan
- utiliser la règle du gamma
- définir oxydant et réducteur
- placer des couples sur une échelle des potentiels rédox
Il faut faire très attention pour les exercices quantitatifs à bien avoir défini le réducteur et l’oxydant et à prendre compte des coefficients …
Principe de résolution des exercices :
- préciser quelle est l’espèce oxydée et l’espèce réduite
- écrire les demi équations concernant chaque espèce
- affecter des coefficients à ces demi-équations pour que leur somme ne laisse apparaître aucun électron libre.
- réaliser la somme des deux demi-équations pour mettre en place l’équation bilan définitive.