Calorimétrie - Chaleur de réaction
1 Définitions
La calorimétrie est l'étude quantitative des transferts d'énergie d'un système à l'autre à l'échelle microscopique en se basant sur la mesure des températures.
Au cours d'une réaction chimique totale, la transformation des réactifs en produits s'accompagne d'un échange d'énergie entre le système {réactifs+produits} et le milieu extérieur. On appelle alors chaleur de réaction, généralement notée Qr effectuée à une pression constante et à une température donnée notée t, la quantité d'énergie qu'elle échange avec le milieu extérieur. On utilise souvent l'unité kJ.mol-1.
La chaleur de réaction est donc l'énergie donnée ou reçue par le système constitué des réactifs pour évoluer vers le système composé des produits, pour une mole de réactifs. Elle résulte finalement d'une variation d'énergie interne du système moléculaire, énergie stockée dans les liaisons à l'intérieur des molécules.
Pour mesurer cette chaleur émise ou reçue, on utilise une " bombe calorimétrique " où l'échange calorimétrique se fait avec des réactifs en quantité connue et une masse m d'eau dont on mesure la température avant et après réaction. N.B. : lorsqu'une réaction peut être considérée comme la combinaison de plusieurs autres réactions, on peut additionner leurs chaleurs respectives.
2 Mise en évidence d'un transfert s'énergie au cours d'une réaction
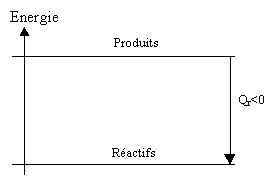
Lorsque la réaction est exothermique, le système {réactifs+produits} cède de l'énergie au milieu. Alors on a Qr<0. En effet, le système constitué par les réactifs évolue vers le système constitué par les produits en perdant de l'énergie qui est transférée au milieu ambiant sous forme de chaleur.
On qualifie ce type de réactions de exoénergétique.
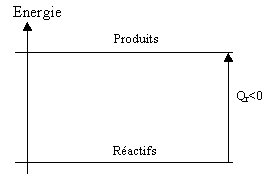
A l'opposé, une réaction est dite endothermique lorsqu'elle implique le fait que le système
{réactifs+produits} reçoive de l'énergie du milieu extérieur. Dans ce cas, on a Qr>0. On l'appelle
aussi endoénergétique, ce qui signifie que le système des réactifs ne peut évoluer vers le système
des produits qu'en recevant de l'énergie du milieu. Cette énergie est obtenue grâce à la chaleur
du milieu.
Le signe de l'énergie transférée est n'en fait pas seulement déterminé en fonction des échanges thermiques visibles. Il est positif si le système reçoit de l'énergie. Ceci peut se manifester de plusieurs façons :
- soit sa température augmente ;
- soit le système change d'état physique ( c'est à dire qu'il passe de l'état solide à l'état liquide ou de l'état liquide à l'état gazeux).
Inversement, il est négatif si le système perd de l'énergie c'est à dire :
- si sa température s'abaisse ;
- si il passe de l'état gazeux à l'état liquide ou de l'état liquide à l'état solide.
Cependant, même si ce n'est pas directement sous forme de chaleur que se manifeste le transfert d'énergie, l'usage veut que l'on désigne l'énergie transférée par " quantité de chaleur ".
3 Propriété des chaleurs de réaction
La quantité d'énergie échangée entre un système chimique et le milieu extérieur est proportionnelle à la quantité de transformation réalisée.
Cette dernière correspond au nombre de molécules de réactifs ayant subit la réaction. On a donc ici comme limite la quantité de réactif limitant disponible.
On appelle réactif limitant le réactif qui est en quantité moindre, relativement aux coefficients stœchiométriques et qui limite donc la réaction.
Par exemple avec A+2B -> C, le réactif limitant n'est pas nécessairement A. Si on a 1 mole de A et 2 de B, les réactifs sont en quantités stœchiométriques et il n'a pas de réactif limitant ( ou ils le sont tous les deux). Si on a 1 mole de A et 1 de B, alors B est le réactif limitant car seule 0, 5 mole de A pourra réagir. Si on a 1 mole de A et 3 de B alors A est le réactif limitant puisque 3 moles de B pourraient réagir avec 1, 5 moles de A.
4 Principe de l'état initial et de l'état final
La chaleur d'une réaction effectuée sous pression constante, à une température donnée, ne dépend que de l'état initial des réactifs et de l'état final des produits.
Cette loi de conservation permet de déterminer la température de réaction.
On peut notamment utiliser un diagramme énergétique qui est la représentation graphique des différents niveaux d'énergie par lesquels passe le système. La chaleur de réaction reviendra à la différence entre l'énergie de départ et l'énergie d'arrivée.
La possibilité de combiner plusieurs réaction est directement applicable dans le diagramme énergétique. On peut l'assimiler à une sorte de relation de Chasles telle que celle qui a été vue en mathématiques depuis la classe de troisième.
5 Les grandeurs caractéristiques de la calorimétrie
On appelle capacité thermique l'élasticité de la température d'un milieu par rapport à l'énergie qui est déversée sur lui. Un milieu de forte capacité thermique est tel que la totalité de l'énergie qui est libérée par une réaction chimique qui a lieu en son sein est répercutée sous forme de chaleur. Si un milieu a une très faible capacité thermique, il aura tendance à garder la même température même si une réaction chimique se déroule et lui transmet beaucoup d'énergie.
On obtient la capacité thermique (notation habituelle c et non K )Kt par le calcul : avec Qr, quantité d'énergie libérée en joules, et les températures finales exprimées en Celsius ou en Kelvin. On obtient donc une grandeur Kt exprimée en J.°C-1 ou en J.K-1.
On utilise parfois une grandeur liée à la précédente : la capacité thermique massique mesure l'énergie ( en joules) qui doit être transférée par une masse unité du système de masse m ( exprimée en kg) pour que sa température varie de 1 °C ou 1 K. Elle s'exprime alors en J.K-1.kg-1.
Le calcul est 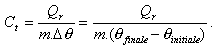
Remarque : Les gaz ont une particularité : leur capacité thermique est fonction du type de transformation qu'ils subissent.
La dernière grandeur utilisée est la chaleur latente du système ( L). Il s'agit de l'énergie microscopique qui doit être transférée par une masse unité du système de masse m pour changer d'état physique à température constante. Avec Q énergie transférée : L'unité est logiquement la J.kg-1.
Le principe zéro de la calorimétrie :
Si un ensemble de système est placé dans un calorimètre, le solde de leurs énergies transférée est nul.
L'énergie dégagée par l'un est nécessairement absorbé par un autre mais on a toujours.
6 Aspects énergétiques des dissolutions
Dissolution des ions
La dispersion des ions est un phénomène endothermique. L'énergie interne du solvant diminue, c'est à dire que l'énergie cinétique microscopique diminue. La température doit baisser.
La solvatation est un phénomène exothermique. L'énergie interne du solvant augmente, c'est à dire que l'énergie cinétique microscopique augmente. La température doit s'élever.
La simultanéité des deux processus libère ou absorbe de l'énergie au total. Suivant la nature du soluté et selon la réaction qui prime, on peut observer une élévation, une diminution ou une conservation de la température globale.
La chaleur de dissolution est l'énergie transférée lors de la dissolution d'une mole d'un composé ionique. Au lieu d'utiliser la bombe énergétique, on étudie tout simplement les variations de la température du solvant de masse m et de capacité thermique massique c.
Pour une mole de soluté, le solvant échange : Le soluté échange
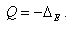 La chaleur
de dissolution est
La chaleur
de dissolution est 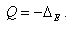
Dissolution des composés moléculaires
La rupture d'une molécule de soluté ou de solvant est endoénergétique.
La formation de nouvelles entités chimique et l'hydratation des ions est exoénergétique.
Le bilan des deux réactions est donc variable : si l'énergie libérée lors de la formation de nouvelles entités chimiques est supérieure à celle consommée par la rupture des molécules, alors il y aura élévation de température.
Ceci peut être vérifié au moyen d'un diagramme énergétique.
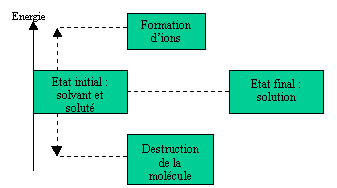
Les énergies libérées et absorbées par le solvant et le soluté sont égales. Dans les hypothèses posées plus haut, on constate effectivement que le transfert d'énergie est à somme nulle. Il n'y a donc pas eu d'énergie communiquée vers l'extérieur de ce système.
On peut par contre considérer que l'énergie créée par formation des ions soit inférieure à
l'énergie absorbée lors de la destruction des molécules. Dans ce cas, on aura le schéma suivant :
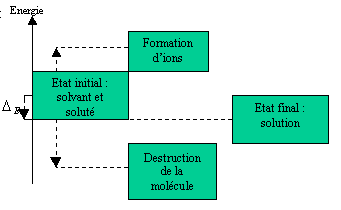
Attention : dans ce cas précis, on respecte toujours le principe zéro de la calorimétrie. Les échanges internes au système ne sont certes pas nuls mais l'énergie consommée par la destruction des molécules et non fournie par la formation des ions est tout simplement captée d'un élément extérieur au système : le milieu.
Les difficultés de la leçon
- Faire attention au signe de Qr et.
- veiller à bien définir le système sur lequel on travaille.